近期,根据联交所公告贝康医疗(2170.HK)获得PGT-A试剂盒三类医疗器械注册证,这一消息让原本平静的国产三代试管PGT-A试剂盒市场再度成为焦点。

作为辅助生殖领域的核心耗材,PGT-A试剂盒直接关系到胚胎检测的精准性与临床诊疗的合规性,而当前市场上贝康、亿康、嘉宝三家头部企业的产品布局,折射出行业在政策监管趋严背景下的发展态势。
在医疗器械监管强化、人类辅助生殖技术规范持续收紧的大环境下,合规已成为赛道竞争的核心标尺,而部分企业的发展现状,也让行业面临着诸多现实拷问。
从行业发展来看,PGT-A试剂盒作为第三代试管婴儿技术的关键支撑,其研发、生产与临床应用始终处于国家强监管体系之下。根据《医疗器械监督管理条例》,三类医疗器械作为最高风险类别,实行“试剂+仪器”配套审批的核心管理逻辑,试剂与配套检测设备的适配性,且设备变更必须完成注册,这是保障检测结果准确性与临床安全性的基础。

同时,《人类辅助生殖技术管理办法》明确要求,开展辅助生殖技术的医疗机构需配备“与开展技术相适应的技术和设备”,且相关设备与试剂均需具备医疗器械合法合规资质,这一要求在卫健委对生殖中心的定期技术评审中,更是成为不可逾越的红线。
在此背景下,贝康医疗此次获批的PGT-A试剂盒,不同于此前的产品,该款试剂盒(国械注准20263400529)明确适配企业自主研发的DA500/DA5000国产高通量测序平台,贝康医疗完成了从“试剂有证”到“国产平台”的升级,其布局既契合了国家对医疗器械国产化的鼓励导向,也完全符合当前三类医疗器械的监管要求,为临床的本地化部署应用提供了稳定、可控的合规选择。
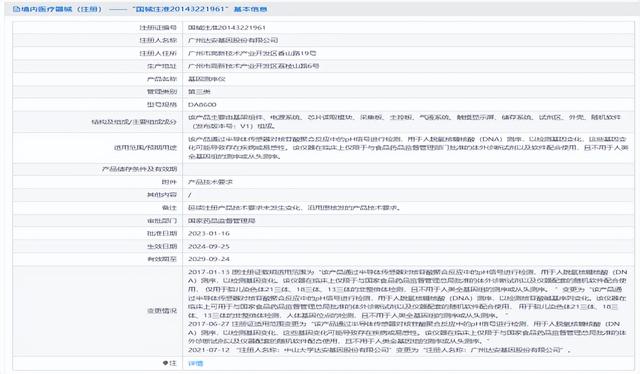
目前,市场上部分已获证的PGT-A试剂盒,其中基于达安基因DA8600(半导体)基因测序仪,但据行业公开信息,该款测序仪已正式停产。从三类医疗器械的试剂和和配套测序仪的监管逻辑来看,平台成为了亟待厘清的问题
另外,还有获得注册证PGT-A试剂盒是Illumina的MiSeqDx测序平台,而2025年商务部已将Illumina列入不可靠实体清单,禁止其向中国出口基因测序仪,这也意味着,使用该试剂盒在其他平台开展检测,将明显违反医疗器械监管相关规定。
根据国家卫健委的要求,开展三代试管技术的生殖中心需接受定期技术评审,评审的核心要点之一,就是核查检测设备、试剂的资质匹配性与合规性,即“人机料法环”的高度统一。若生殖中心使用配套平台已停产、或未完成注册变更的试剂盒,在评审中必然面临资质核查不通过的结果,轻则被扣分整改,重则可能被暂停相关技术服务资质。
近年来,国家对辅助生殖领域的监管力度持续加大,从严控非法性别鉴定到规范技术服务流程,合规已从医疗机构的“加分项”变为“生死线”,这也让下游机构在选择试剂盒产品时,不得不将合规性放在首位,部分打着科研旗号的不合规产品,将给临床和患者带来风险,为中国人口战略的发展守住底线。
免责声明:所有平台仅提供服务对接功能,资讯信息、数据资料来源于第三方,其中发布的文章、视频、数据仅代表内容发布者个人的观点,并不代表泡财经平台的观点,不构成任何投资建议,仅供参考,用户需独立做出投资决策,自行承担因信赖或使用第三方信息而导致的任何损失。投资有风险,入市需谨慎。

 迁址公告
迁址公告
 古东管家APP
古东管家APP
 关于我们
关于我们
请先登录后发表评论